摘要: 前几日因任务关系需要在数据库中找一些关于胃癌临床样本的芯片数据,在耗费几滴珍视明后,竟被我找到一个非常不错的数据集。这个数据集(GSE27342)的样本来源于80名胃癌患者,并分别对肿瘤组织和瘤旁组织进行了检测。检测这批样本的基因芯片平台是Affymetrix公司的Exon 1.0 芯片。原数据的收集者运用这批芯片数据发表了两篇分数不太高并且内容相似的文章,说实话这实在是有点可惜!闲话少说,现在我来讲述一下我是如何分析这批...
前几日因任务关系需要在数据库中找一些关于胃癌临床样本的芯片数据,在耗费几滴珍视明后,竟被我找到一个非常不错的数据集。这个数据集(GSE27342)的样本来源于80名胃癌患者,并分别对肿瘤组织和瘤旁组织进行了检测。检测这批样本的基因芯片平台是Affymetrix公司的Exon 1.0 芯片。原数据的收集者运用这批芯片数据发表了两篇分数不太高并且内容相似的文章,说实话这实在是有点可惜!闲话少说,现在我来讲述一下我是如何分析这批数据的。
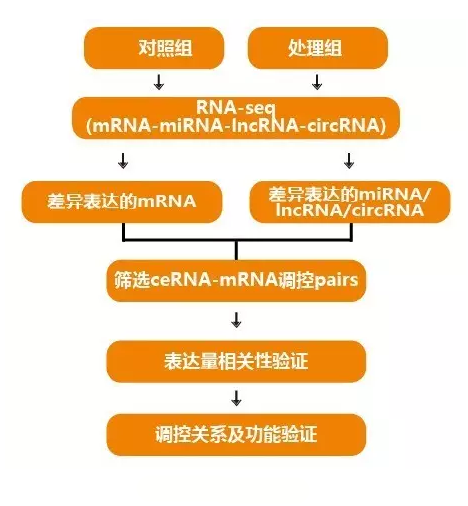
首先借助于GCBI强大的数据抓取能力,直接将这160个样本的芯片原始数据导入到GCBI在线分析实验室。数据拿到手后,接下来要做的就是如何对样本进行分组并预设分析目标了,这是分析数据前最关键的工作。虽然这80对检测样本还有其他临床分组信息,比如患者年龄、肿瘤分期等,不过我很自然地先选择先将样本分为肿瘤样本与瘤旁样本,然后分析这两组间的数据。很简单,因为这是这批数据最主要、最核心、而且最简便的分组信息。在选择好分组方式后,根据待分析的两组样本的特征和预设的分析目标设计了一个经典的数据分析流。具体分析流程请见下图:
设计好数据分析流后,点击保存并运行,接下来要做的是起身泡杯茶或者上趟厕所(隐约好像哪里有点不对),因为几分钟后就要分析繁复的结果了。数据分析完成后,我大致瞟了眼差异结果,没有细看。单独的差异基因数据其分析的重要性其实并不太大,只要知道大概有多少差异基因,样本分类好不好就可以。之前我预想的是期望通过这批数据找到与胃癌相关的癌基因或抑癌基因,所以我把主要的精力放在了信号通路分析结果上,希望能通过它先找到一些与肿瘤相关的关键通路和基因。在204个通路结果中有不少与肿瘤有关系,其中排在前面的是PI3K-Akt信号通路(涉及到了80个差异基因!)。经过与差异结果进行比对后发现,PI3K-Akt通路中COL1A1基因的差异倍数最大。
这是个什么鬼?没见过啊!搜索后才发现原来是编码Ⅰ型胶原蛋白的基因。
这胞外基质蛋白啊!再多看一眼上面那张表,好多都是表达细胞外基质的基因。我是来找癌基因的啊!怎么会是这么个结果,好心塞……在喝完1/3口咖啡后,一道闪电划过带走了一个本来就所剩无几的脑细胞:这可能说明细胞外基质在胃癌的发生、恶化和转移过程中起着比较重要的作用!这属于肿瘤细胞的微环境研究范围了。胞外基质、组织液、微血管和其他细胞一起构成了肿瘤微环境。有点类似于人类社区,肿瘤细胞所处的微环境为其增殖、发育和转移提供了必要的物质条件和信息交流。
有了这个设想之后,还需要再看看能不能通过其他分析结果进行印证。首先我看的是基因信号转导网络,因为这个网络是基于数据库已有的基因间关系作出的,关系网中的基因间调控关系都是经过验证的,比较可信。下面是基因间信号转导网络的局部图,这张图反映了在胃癌细胞中有大量表达细胞外基质的基因发生了差异表达,这些基因的差异表达最终表现为其产物——细胞外基质——在肿瘤细胞外的丰度和结构发生了异常。
数据分析结果中还有一个基因间共表达网络,这个结果是不是也能反映细胞外基质的重要性呢?
不负我心,果然,基因共表达的结果也十分支持我的假设。至此,我预判细胞外基质肯定与胃癌相关。接下来要做的就是用实验来验证这一假设,正准备撸起袖子准备大干一场的时候,才发现实验室和初恋一起离开我好多年了。既然自己做不了实验,那就看看其他人是如何做细胞外基质实验的。
用GCBI搜索了一番,没有找到关于胃癌细胞外基质研究的好文章,不过有篇验证Ⅰ型胶原蛋白促进乳腺癌恶化和转移的文章:Matrix crosslinking forces tumor progression by enhancing integrin signaling。Cell的,值得拥有!
本文由 GCBI学院 作者:其明技术专家 发表,转载请注明来源!

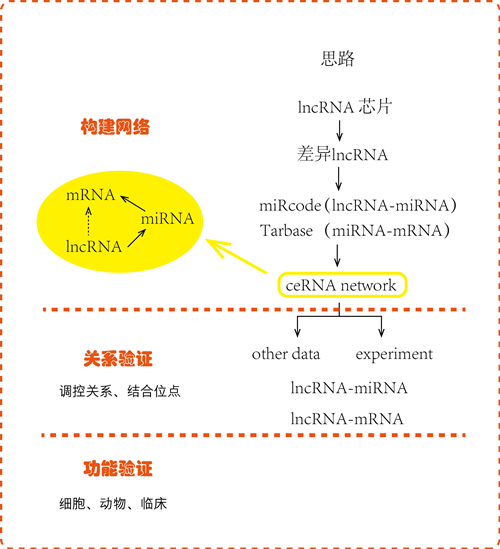


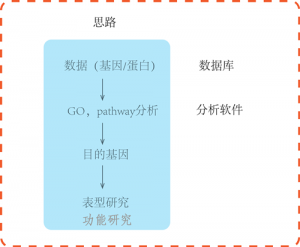


作为一名临床博士,如果能够熟练学习这些方法,将会为我们开辟新的研究路线
刚刚临床博士毕业,目前没有实验条件,正好学上
很好,谢谢,这还是很有用的